骨修复机制研究 Tissue Cytometry技术*助力免疫调控分析
来源:缇基(北京)科技有限公司
发布时间:2026-05-07 11:53:03
骨缺损是临床上的一大难题,这主要是由于骨骼的自我修复能力有限,且传统治疗方案存在较高的并发症风险。传统组织工程方法通常依靠膜内成骨实现骨修复,但该方法的治疗效果往往欠佳。本研究发现,人诱导多能干细胞来源的软骨细胞膜片可通过免疫刺激被激活,在体内启动软骨内成骨过程。基于这一发现,我们推测在骨缺损修复中,以软骨为基础的材料可能在诱导成骨方面具有更好的效果。
人血小板裂解液是一种高、易于获取的生物活性分子来源,富含多种生长因子和功能蛋白,在再生医学领域展现出巨大的应用潜力。

上海交通大学医学附属第六人民医院团队在Advanced Healthcare Materials发表题为” Platelet Lysate–Enriched Human Induced Pluripotent Stem Cell–Derived Chondrocyte Sheets for Bone Defect Repair via Endochondral Ossification”文章。
本研究开发了一种制备人血小板裂解液增强型人诱导多能干细胞来源软骨细胞膜片(iCDCHs)的新方法。实验结果表明,血小板裂解液处理可显著增强软骨细胞膜片的软骨内成骨能力,加速骨再生进程。与同种异体骨移植相比,该细胞膜片能改善骨修复效果,且免疫原性显著降低。
进一步分析发现,该软骨细胞膜片通过激活磷脂酰肌醇 3 - 激酶 / 蛋白激酶 B 信号通路促进 M2 型巨噬细胞极化,进而产生多种促再生代谢因子,构建出利于骨缺损高效修复的微环境。上述研究结果表明,人诱导多能干细胞来源的软骨细胞膜片在骨缺损修复中具有良好的应用前景,可作为组织工程领域中同种异体骨移植的一种重要替代方案。
实验部分
1. 免疫荧光染色样本的高分辨率成像
研究在探究 iPSC 衍生软骨细胞膜片(iCDCHs/iCDCs)对巨噬细胞极化的影响时,对大鼠股骨缺损组织进行了免疫荧光染色(标记分子包括 iNOS、CD206、DAPI 等,分别对应 M1 巨噬细胞、M2 巨噬细胞及细胞核)。此时借助TissueFAXS 平台,以 20× 放大倍数对染色切片进行扫描成像,清晰捕获了骨缺损部位不同表型巨噬细胞的分布特征,为后续观察 M1/M2 巨噬细胞的数量变化提供了高质量的图像基础。
2. 关键分子表达的定量分析
免疫荧光成像的核心价值在于量化验证。研究通过StrataQuest 软件对染色样本进行定量分析,具体评估了 iNOS(M1 巨噬细胞标志物)和 CD206(M2 巨噬细胞标志物)的表达水平。结果显示,iCDCHs 组骨缺损部位 CD206⁺细胞占比显著升高(27.95%),而 iNOS⁺细胞占比显著降低(1.41%),直接证实了 iCDCHs 能诱导巨噬细胞从促炎 M1 表型向抗炎 M2 表型极化 —— 这一量化数据是支撑 “免疫调控微环境促进骨再生” 机制的核心证据。
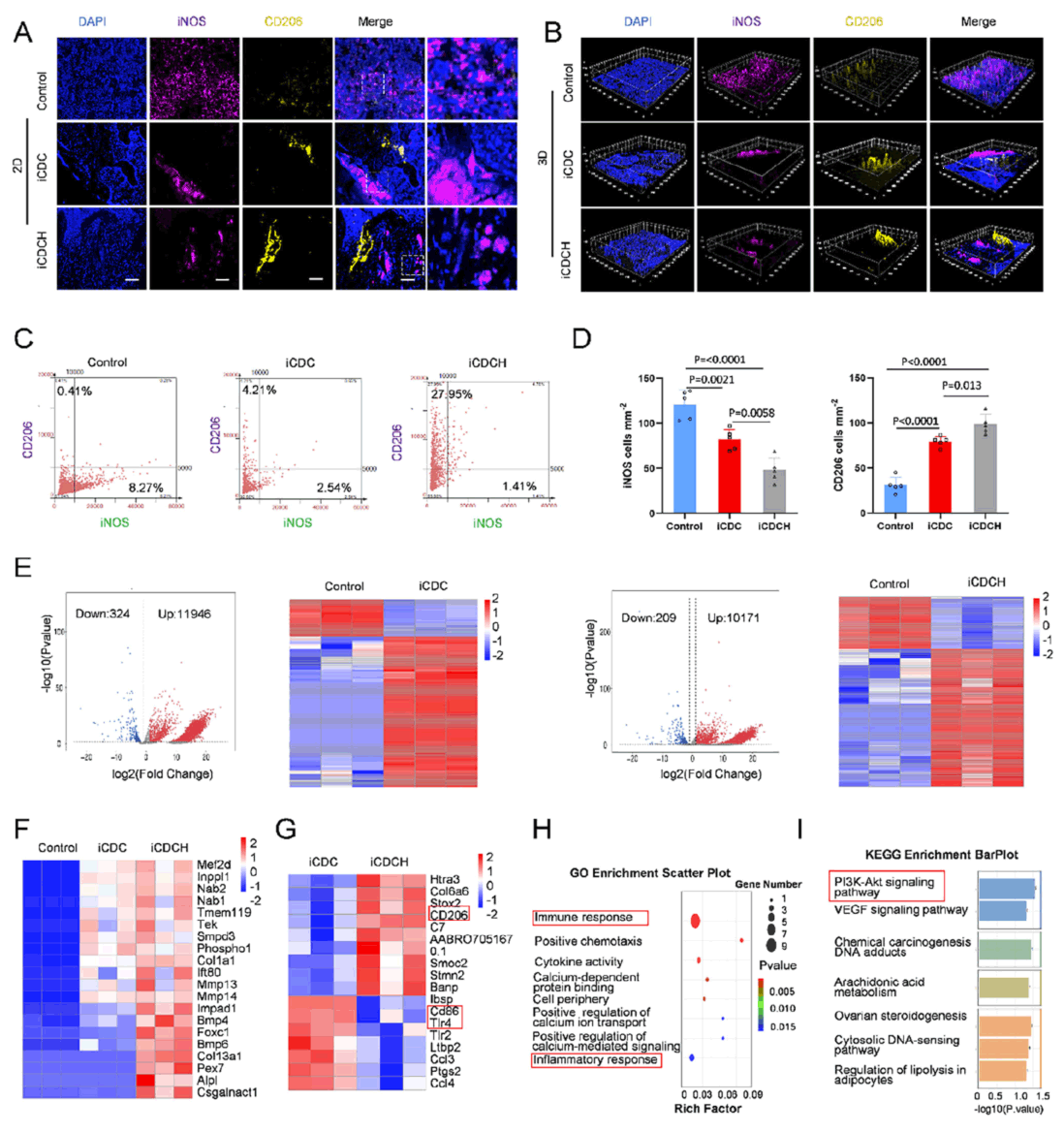
Figure 4 组织学与转录组学分析
温馨提示:为规避购买风险,建议您在购买产品前务必确认供应商资质及产品质量。
